Retour accueil | Droit de copies | Sommaire de ce dossier | Page Précédente |
Comment évaluer les incertitudes en analyses (bio)chimiques. Une introduction à l'aide d'un exemple simple : l'étalonnage d'une solution d'acide chlorhydrique de concentration voisine de 0,1 mol/L par pesée(s) d'hydrogénocarbonate de potassium pur et anhydre. Suite ...
3. Construction d'un tableau de calcul de résultat d'étalonnage avec l'incertitude-type
Dans le cas du protocole avec détermination du volume équivalent après enregistrement de la courbe pH = f(volume d'HCl versé).
On rappelle la relation pratique de l'étalonnage
qui va permettre la construction du tableau de calcul (cf. page précédente) :
C = [ 2 * (mc * t) / M] * (1/Vb) * r
Avec, par exemple, C en mol/L ; mc en g ; M en g/mol ; Vb en L.
Et r le facteur global de répétabilité. r = 1 (sans unité) mais avec une
incertitude-type u(r).
Et t le titre du carbonate de sodium (m/mc) .
mc,f, M, Vb et r sont des variables indépendantes.
On suppose une manipulation d'étalonnage qui a mis en oeuvre une pesée de 0,0946 g et a conduit à une valeur Vb = 18,02 mL.
A ce stade de l'étude, le tableau de calcul est construit en se contentant de collecter toutes les valeurs de variables et d'incertitudes-types et d'appliquer la relation pratique de l'étalonnage telle que présentée ci-dessus :
| Symbole de variable | Explicitation de la variable | Valeur (x) | Incertitude-type u(x) |
| r | répétabilité | 1 |
0,001 |
| mc | masse pesée (conventionnelle) |
0,0946 g | 0,000 13 g |
| t | titre | 0,9997 |
0,000 4 |
| M | masse molaire du carbonate de sodium |
105,98844 g |
0,000 69 g |
| Vb | volume pour l'équivalence acido-basique |
18,02 10-3 L |
0,013 10-3 L |
| C | Concentration en HCl (le résultat)) |
0,099 032 5 mol/L |
Il s'agit maintenant de déterminer u(C). Comme la formule pratique de l'étalonnage ne fait intervenir que des produits ou des quotients et que les variables sont indépendantes, on va utiliser la formule suivante :
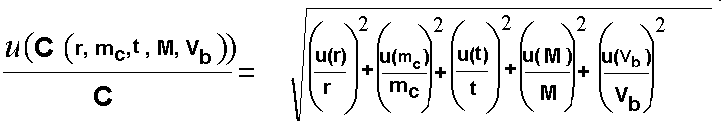
|
On va donc ajouter une colonne supplémentaire au tableau de calcul pour déterminer les u(x)/x pour chacune des varaiables r, mc, f, M, Vb, puis finalement u(C)/C.
Page mise à jour 07-12-2002 -- JF Perrin -- | Retour accueil | Droits de copies | Sommaire de ce dossier | Page Précédente |
Date de consultation : 25-05-2026