Retours vers :
[Accueil]
[Sommaire du dossier]
JF Perrin mise à jour 2007/2017
[A propos de l'auteur]
[Droits de copie]
![]()
Dans une solution tampon, puisqu'on a la relation \( pH = pK_{\text{a}} + \log {\frac {[B^{-}]}{[AH]}} \), on peut penser que calculer une recette exacte de tampon de pH est simple.
Il suffirait, au moins dans un premier temps, de calculer [AH] et [B-] solution du système :
\( \left\{ \begin{array}{11} pH = pK_{\text{a}} + \log {\frac {[B^{-}]}{[AH]}} \\ [B^{-}]+[AH] = c_T \end{array} \right. \)
Où AH désigne la forme acide et B- la forme base du couple ; et cT la concentration du tampon.
Les données classiques de la littérature chimique donnent les pKa des couples acide/base à 25°C et à dilution infinie (force ionique nulle). On parle de pKa thermodynamique. Malheureusement, un calculateur de tampon qui calcule un tampon avec cette seule donnée ne conduira qu'à des recettes de fabrication très approximatives. En effet, pKa dépend de la température et de la force ionique de la solution : pKa dans les conditions du tampon peut être assez éloigné du pKa thermodynamique. On trouve malheureusement beaucoup de tels calculateurs en ligne. Il faut les éviter.
Un bon calculateur de tampon utilise des équations sophistiquées qui lui permettent d'aboutir à la valeur exacte du pKa aux conditions réelles du tampon
dont il faut établir la recette de fabrication (pour la température choisie
et en calculant la force ionique qu'il y aura). Il existe des versions commerciales. A ma connaissance il n'existe qu'un seul bon calculateur libre en ligne, celui de
Rob Beynon (Université de Liverpool). Il est disponible à :
https://www.liverpool.ac.uk/buffers/buffercalc.html
ou à
https://www.bioinformatics.org/JaMBW/5/4/index.html
ou à
http://www.biomol.net/en/tools/buffercalculator.htm.
Soit à commander un tampon Tris-Cl pH 8,2 à 37°C et 0,1 mol/L.
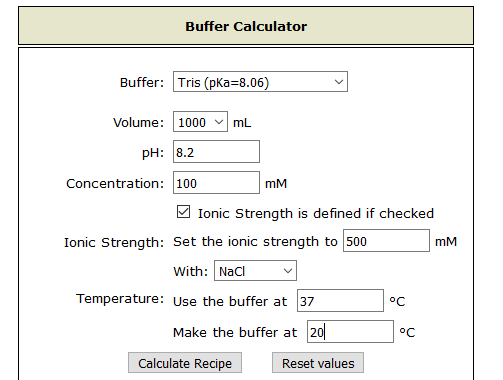
On renseigne le formulaire de "commande"
On lance le calcul. Le calculateur retourne des résultats et des recettes de fabrication.


Commandons le même tampon Tris-Cl 0,1 mol/L pH 8,2 à 37°C mais de force ionique élevée à 500 mol/L par NaCl.