Retours vers :
[Accueil]
[Sommaire du dossier]
JF Perrin mise à jour déc. 2015-2019
[A propos de l'auteur]
[Droits de copie]
![]()
Les acides aminés font partie de la catégorie dite des métabolites primaires.
Leur production répond à 3 types d'utilisation :
agents de saveur en alimentation humaine : ainsi le glutamate agent de saveur de type "goût de bouillon"
agents édulcorant (pouvoir "de goût sucré") en nutrition humaine : ainsi l'aspartam est un édulcorant fabriqué par condensation à partir d'asparagine et de phénylalanine
agents de complémentation en nutrition humaine et animale : pour le cas des acides aminés essentiels. On rappelle que les acides aminés essentiels aux porcs, volailles, lapins et humains comme la méthionine et la lysine sont généralement (à l'exception notable du soja) insuffisants chez les végétaux.
La lysine est l'un des 4 acides aminés essentiels majeurs de l'alimentation humaine et animale. Les souches productrices appartiennent au genre Brevibacterium et Corynebacterium. Les souches utilisées sont des mutants sophistiqués.
L'étude de la voie biologique de biosynthèse de la lysine et de sa régulation va permettre de comprendre comment on a pu obtenir des souches mutantes hyperproductrices de lysine et sécrétoires (une qualités a priori peu compatible avec la bonne économie physiologique des cellules) : on a abouti à des mutants avec une voie de biosyntrhèse mal régulée : "rétroinhibition perdue" et/ou absence de répression anabolique.
Les mutants hyperproducteurs sont :
L'étude fine des flux des métabolites et du NADPH associée aux techniques de génie génétique permettent de créer des superproducteurs bien plus sophistiqués et subtils que ce qui est écrit ci-dessus ...
Certains mutants producteurs ont été obtenus grâce à la technique du crible de résistance à un analogue de la lysine (la S-2-aminoéthylcystéine). En présence de S-2-aminoéthylcystéine, analogue de la lysine, une souche normale voit la chaîne de biosynthèse de la lysine rétroinhibée et réprimée : elle ne cultive pas ou très mal sur un milieu synthétique plus analogue dépourvu de lysine alors qu'elle est lysine+. Un mutant dérégulé de phénotype [lysine+] synthétise la lysine en présence de l'analogue : il cultive sur le milieu sans lysine + analogue.
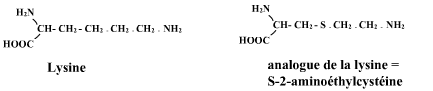
Les milieux des cultures industrielles sont généralement à base de mélasses, d'ammonium, plus les sels minéraux. Ils sont enrichis en biotine et thiamine. La teneur des métabolites essentiels qui comblent les auxotrophies est très strictement optimisée notamment la teneur en méthionine et thréonine. Les milieux industriels sont des "secrets de fabrication".
Ce qui suit est tiré de de Q. Hua, C. Yang, K. Shimuzu, Metabolic control analysis for lysine synthesis using Corynebacterium glutamicum and experimental verification, Journal of Biotechnology and Bioengineering (2000) vol. 90 N° 2, 184-192.
• La souche utilisée: C. glutamicum ATCC21253-pJC33, souche dérégulée productrice de lysine : auxotrophe pour la thréonine et la méthionine (homosérine deshydrogénase déficiente) et aussi la leucine et superproductrice d'aspartokinase (grâce à un gène porté par le vecteur pJC33). Comme expliqué au paragraphe 2 ci-dessus.
• le milieu de culture (pour 1 L) : (A) 75 g glucose, 1 g citric acid, 0.6 g MgSO4,7H2O, 50 mg FeSO4,7H2O, 2 g NaCl, 1 g CaCl2 and 20 ml concentrated salts solution, adjusted to pH 4.0 with HCl; (B) 4 g K2HPO4, 2 g KH2PO4, 733 mg threonine, 1.5 g leucine, 600 mg methionine, 1 mg biotin, 2 mg thiamine,HCl and 40 g (NH4)2SO4. The compositions of concentrated salts solution were: 200 mg/L FeCl3,6H2O, 200 mg/L MnSO4, 50mgl ; ZnSO4,7H2O, 20 mg/L ; CuCl2,2H2O, 20 mg/L ; Na2B4O7,10H2O and 10 mg/L (NH4)6Mo7O24,4H2O, adjusted to pH 1.5 with HCl.
On notera la présence de thréonine, leucine et méthionine dans le milieu de culture : souche dérégulée productrice de lysine auxotrophe pour ces 3 aminoacides comme exposé au paragraphe 2.
• Le procédé. Un procédé "batch" très classique. "The pH value of the medium was was monitored and controlled at pH 7.0 by the addition of 25% w/w ammonium hydroxide. The fermentation temperature was controlled at 30°C. The dissolved oxygen concentration was monitored [...] and controlled to 5% of air saturation.
Avec le milieu proposé, le glucose est source de C (pour la croissance, pour les pertes liées à la maintenance et pour la biosynthèse dérégulée de lysine) et d'énergie (régénération d'ATP et de pouvoir réducteur NADPH pour la croissance, pour la maintenance et pour la biosynthèse dérégulée de lysine). Il apparaît clairement que le rendement de conversion du glucose en lysine est le plus médiocre pendant la phase de croissance active (<0,09 g de lysine par g de glucose). C'est assez évident : en phase de croissance, il y a bien sûr les besoins (faibles) pour la maintenance des bactéries mais surtout beaucoup de glucose est utilisé comme source d'énergie et source de C pour fabriquer de la biomasse. Ce glucose là n'est pas dirigé vers la biosynthèse de lysine. Quand la croissance est quasi arrêtée ou arrêtée, la dérégulation de la voie fait que le glucose n'est plus consommé que pour les besoins (faibles) de maintenance des bactéries et pour les besoins de la voie dérégulée de biosynthèse de la lysine. Le rendement de conversion est donc a son maximum dans les conditions proposées.
On peut calculer la productivité horaire volumique globale du réacteur pendant son temps de fonction : 14 g/L en lysine en 35h soit PVH = 0,4 g-1h-1. Le rendement global de conversion du glucose en lysine sur les 35h de production est de 14/85 = 0,16 g de lysine par g de glucose.
Les milieux des cultures industrielles sont généralement à base de mélasses, d'ammonium, plus les sels minéraux. Ils sont enrichis en biotine et thiamine. La teneur des métabolites essentiels qui comblent les auxotrophies est très strictement optimisée notamment la teneur en méthionine et thréonine. Les milieux industriels et les procédés sont des "secrets de fabrication". Il est quasi impossible d'obtenir de leur part des données vraiment exploitables.
Chez Corynebacterium glutamicum on aurait pu obtenir des rendements industriels de conversion du glucose en lysine de plus de 0,45g de lysine par g de glucose consommé.
Pour ceux qui veulent aller plus loin ...
Si on réalise l'expérience de pensée qui consiste à imaginer une souche aérobie cultivant sur glucose et ammonium et dont la totalité du glucose serait détourné vers la seule production de lysine (c'est évidemment imaginaire, il faut un minimum de glucose "détourné" vers la maintenance cellulaire, le turn-over minimal des macromolécules).
En examinant la voie de biosynthèse, le bilan matière et redox à partir du glucose et de l'ammonium, sera donné par exemple par :
C6H12O6 (glucose) + 2 NH3 + 2 Coenz.réduitH2 + n ATP
|
|
|
V
C6H14O2N2 (lysine) + 4 H2O + 2 Coenz.oxydé + n ADP + n phosphates
D'où une proposition de rendement stoechiométrique à Ylys/glu = 1/1 = 1 mol/mol soit 146/180 = 0,81 g de lysine par g de glucose. Une valeur majorée puisque la régénération d'ATP et de pouvoir réducteur, nécessaires à la biosynthèse, impliquent la consommation de glucose !
Sachant que le glucose, source de C, contient 6C et la lysine 6C. Il était évident que le rendement plafond (majoré) de conversion ne pouvait être que de 1 mol de lysine pour 1 mol de glucose.
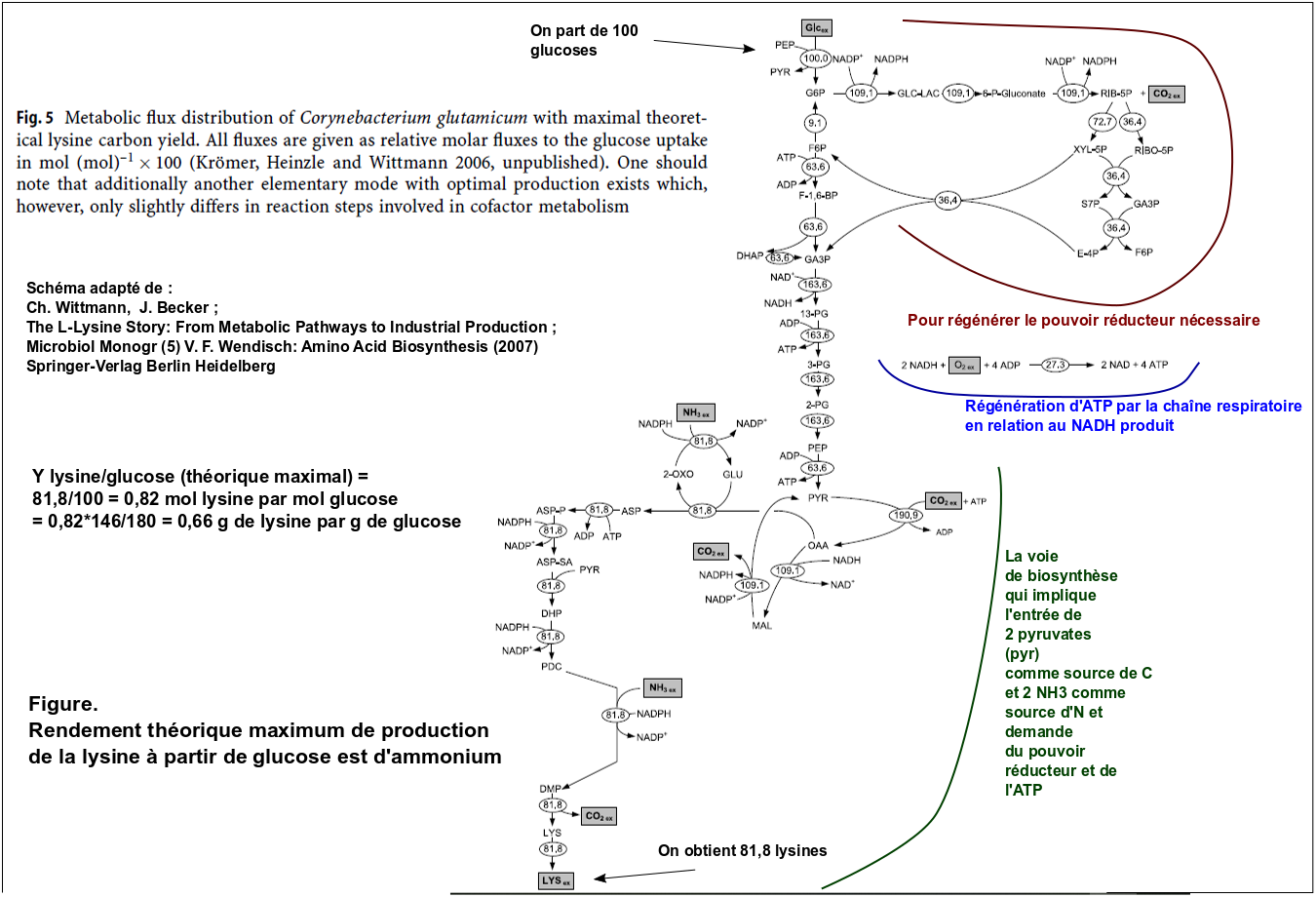
En analysant très finement le réseau de réactions métaboliques impliquées dans la biosynthèse de la lysine, donc en tenant compte des besoins énergétiques (ATP et pouvoir réducteur NADPH), impliqués par la voie de biosynthèse, le rendement théorique maximum de production de la lysine à partir de glucose et d'ammonium s'établit à un peu moins de 0,82 mol de lysine par mol de glucose soit 0,82*146/180 = 0,66 g de lysine par g de glucose. Il faut bien se rappeler ce que signifie ce rendement : on imagine une bactérie qui ne ferait que de la lysine, sans même assurer sa maintenance ! La figure ci-dessous, adaptée de "Ch. Wittmann, J. Becker ; The L-Lysine Story: From Metabolic Pathways to Industrial Production ; Microbiol Monogr (5) V. F. Wendisch: Amino Acid Biosynthesis (2007) Springer-Verlag Berlin Heidelberg " montre cette analyse complexe.