Retours vers :
[Accueil]
[Sommaire du dossier]
JF Perrin mise à jour 2012-2020
[A propos de l'auteur]
[Droits de copie]
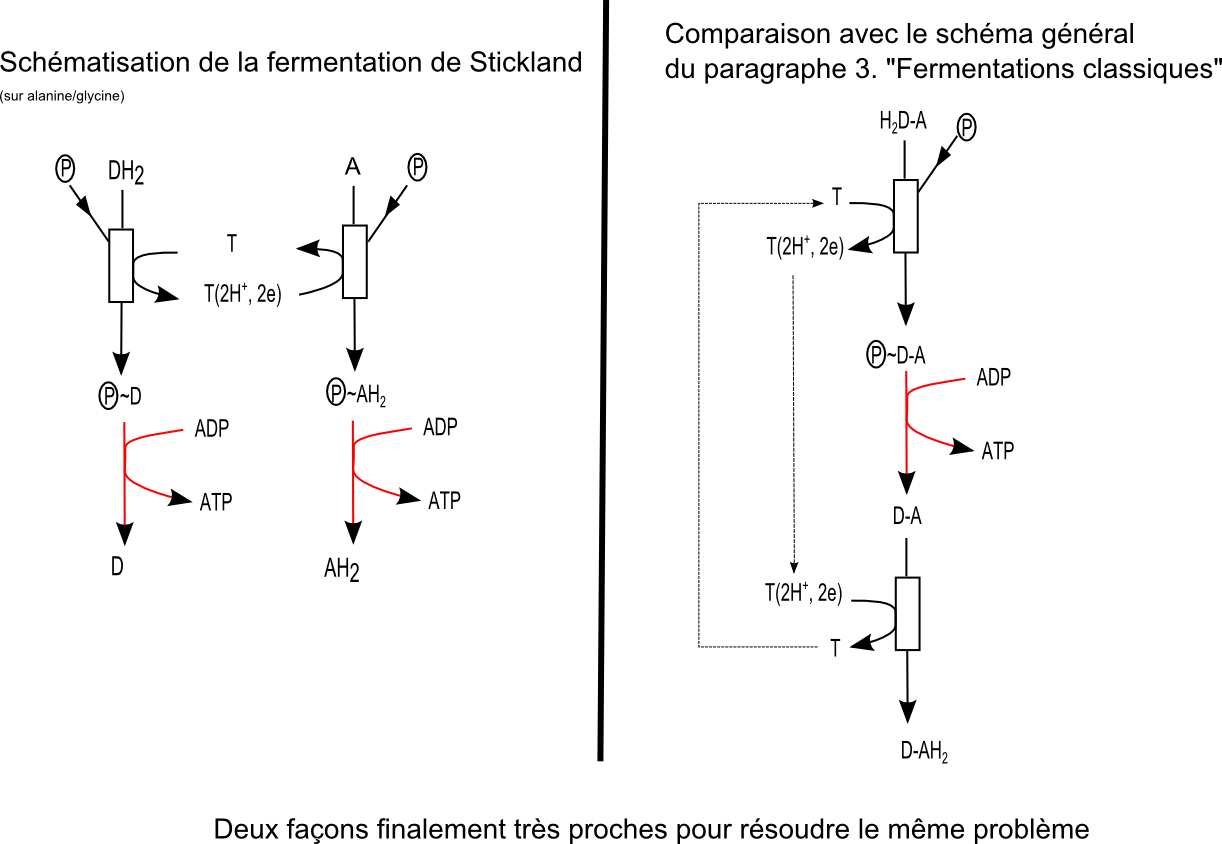
Si les sucres sont les "rois" des substrats fermentescibles, les acides aminés sont de bons substrats de fermentation pour de nombreuses bactéries. Les bactéries du genre Clostridium s'en sont d'ailleurs fait une spécialité. Les systèmes de fermentation des acides aminés sont très divers. Voici la présentation de la voie dite "réaction de Stickland" (rencontrée chez de nombreux Clostridium) et appliquée ici aux 2 acides aminés alanine et glycine.
Cette voie de fermentation est finalement très classique : des composés à haut potentiel d'hydrolyse sont obtenus grâce à l'énergie libre de réactions redox ; L'ATP est régénéré par phosphorylations au niveau du substrat ; le NADH qui dérive de l'oxydation du donneur d'éléctrons (un acide aminé donneur) doit être recyclé grâce à la réduction d'un accepteur d'électron (un acide aminé accepteur).

Il existe d'autres couples donneur/accepteur que le couple alanine/glycine. Ainsi les acides aminés histidine, leucine, valine sont de bons donneurs d'électrons (seront oxydés) tanndis que les acides aminés arginine, histidine, tryptophane sont de bons accepteurs (seront réduits).
Et un schéma de comparaison pour finir :