Retours vers :
[Accueil]
[Sommaire du dossier]
JF Perrin mise à jour 2010-2022
[A propos de l'auteur]
[Droits de copie]
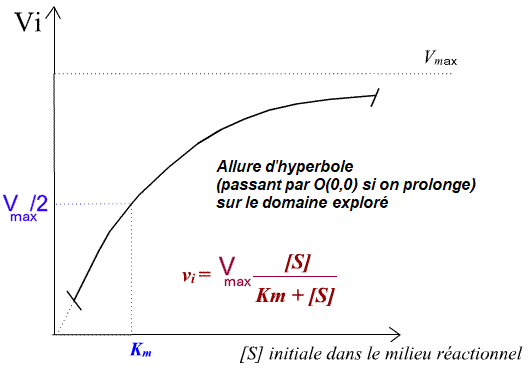
Une enzyme donnée, lors de l'observation de la catalyse d'un substrat observé S en produit observé P selon des conditions qui correspondent à celles décrites dans le paragraphe "Notion expérimentale de vitesse initiale" possède un comportement Michaélien si la courbe expérimentale vi = f([S]) conduit à une portion d'hyperbole d'équation :
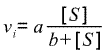 avec a et b ∈ ℝ*+
avec a et b ∈ ℝ*+
qu'on préfère écrire : 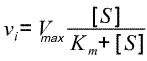 (la forme classique dite équation de Michaelis-Menten)
(la forme classique dite équation de Michaelis-Menten)
qu'on peut aussi écrire : 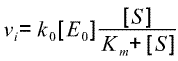
Avec les remarques suivantes :
- vi est la vitesse initiale de réaction ;
- [S] représente la concentration initiale en substrat "observé" dans le milieu de catalyse ;
- le coefficient noté Vmax (Vmax ou V, selon les recommandations UIBMB) est la valeur asymptote de vitesse initiale, on parle par abus de langage de vitesse maximale (L'UIBMB accepte l'utilisation du terme vitesse maximale mais lui préfère celui de vitesse limite - limiting rate. C'est bien meilleur comme terme, mais malheureusement moins usité). Toutes choses égales par ailleurs (température, concentration en substrat, nature du milieu réactionnel ...), Vmax est proportionnelle à la concentration totale en enzyme dans le milieu réactionnel ([E0]). On a ainsi Vmax = k0 [E0]. k0 est appelé coefficient catalytique (ou "constante" catalytique bien qu'il ne soit effectivement constant que dans des conditions opératoires données). k0 s'exprime donc en temps-1 (s-1 par exemple). L'UIBMB autorise les 2 notations k0 et kcat pour le coefficient catalytique ;
- le coefficient Km est appelé coefficient ou "constante" de Michaelis (noté souvent KM mais Km est la notation UIBMB). Km a la dimension d'une concentration en substrat S (en mol/L par exemple). On remarque que pour [S] = Km, vi = Vmax /2. L'UIBMB utilise les 2 appellations possibles synonymes "constante de Michaelis" et "concentration de Michaelis".
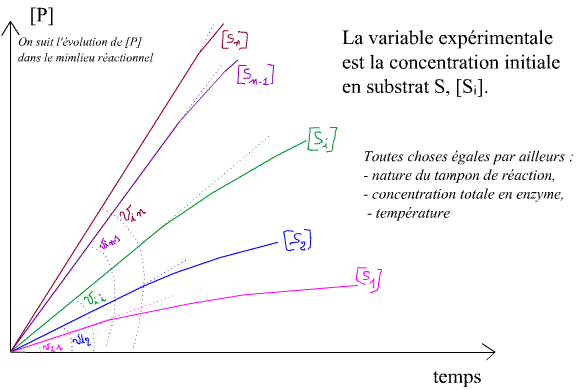
Expériences qui permettent de construire :
On peut aussi regarder ce qui se passe par rapport à la variable [E0], la concentration en enzyme totale (toutes choses égales par ailleurs : concentration en substrat, température ...)

